9月19日-21日,2020 年欧洲肿瘤内科学会(ESMO)年会在线上虚拟召开,在疫情之下继续为改善癌症患者诊疗提供最新前沿进展。百济医学事务部对ESMO 2020肝细胞癌领域的主要进展进行了节选汇编,并特别邀请到东部战区总医院刘秀峰教授进行深入点评,以期对肝癌的临床决策有所启迪。

教授
刘秀峰
东部战区总医院秦淮医疗区肿瘤内科
副主任/主任医师
CSCO理事/副秘书长
CSCO肝癌专家委员会秘书长
CSCO胆道肿瘤专家委员会副主任委员
CSCO胰腺癌专家委员会委员
局部治疗HAIC大放光彩,或成为联合治疗具有前景的新搭档
981O - (HAIC) with , , and () (TACE) for (HCC): A phase III trial
该研究是今年ESMO唯一入选的肝癌口头报告,是由中山大学肿瘤医院石明教授牵头的随机、多中心、开放标签III期临床研究。在这项试验中,患有原发性不可切除HCC肿瘤、最大直径≥7 cm、无大血管侵犯或肝外扩散的成人(≥18岁)患者1:1随机接受肝动脉灌注化疗HAIC(通过重复导管插入术给予方案:奥沙利铂130 mg/m2,亚叶酸钙400 mg/m2,第1天氟尿嘧啶推注400 mg/m2,输注氟尿嘧啶2400 mg/m2持续24小时,每3周1次,直至6个周期)或TACE(表柔比星50 mg,洛铂50 mg,碘油和聚乙烯醇颗粒)。主要终点为OS,次要终点ORR、、PFS( v1.1和)和安全性。
共有315例患者随机接受HAIC(n = 159)或TACE(n = 156)。数据分析截止至2020年4月,患者随访正在进行中。接受HAIC的患者mOS高于TACE:23.1个月(95%CI,18.23-27.97)vs 16.07个月(95%CI,14.26-17.88);HR,0.58(95%CI,0.45-0.75;P < 0.001)。与TACE组相比,HAIC组患者的ORR更高(:45.9[73]vs. 17.9%[28],P < 0.001;:48.4[77]vs. 32.7%[51],P = 0.004),中位PFS更长(9.63[95%CI,7.40-11.86]vs. 5.40[95%CI,3.82-6.98]个月;P< 0.001)。与TACE组相比,HAIC组有更多患者接受后续切除(23.8%[38]vs. 11.5%[18],P = 0.004)。TACE组严重不良事件的发生率高于HAIC组(30 vs 19%,P = 0.03)。
在不可切除HCC患者中,与TACE相比,HAIC联合显著改善了OS。
984P - plus Alone for with Major Vein Tumor (Vp3/4): A Phase II Trial
索拉非尼一线治疗晚期HCC伴PVTT生存获益有限。该项单中心、随机II期研究探索了索拉非尼联合HAIC治疗晚期HCC伴重度PVTT(Vp3/4)的疗效和安全性。共入组了64例既往未接受过化疗或放疗的患者,按照1:1随机接受索拉非尼(400 mg,每日2次)联合HAIC(奥沙利铂35 mg/m2给药2h,第1-3天5-氟尿嘧啶600 mg/m2给药22h,每4周一次)或索拉非尼(400 mg,每日2次)。主要终点为OS,次要终点包括根据评价的ORR、PFS和安全性。
索拉非尼-HAIC组的中位OS为23.5个月(95%CI:10.2-36.8),索拉非尼组为6.8个月(95%CI:4.8-8.8)(P < 0.001)。索拉非尼-HAIC组观察到更高的ORR(16例[57.1%]vs. 1例[4.0%],P < 0.001),更长的中位PFS(10.7个月[95%CI:4.1-17.3]vs. 2.5个月[95%CI:1.3-3.7],P < 0.001)。最常见的3级或4级治疗相关AE为胃肠道反应(7例[21.9%]vs. 6例[18.8%])、手足综合征(6例[18.8%]vs. 2例[6.2%]),血液学异常(4例[12.5%]vs. 0)和肝功能损伤(2例[6.3%]vs. 1例[3.1%])。未发生给药相关死亡。
对于HCC伴严重PVTT患者,与索拉非尼相比, HAIC联合索拉非尼显著改善了生存期,且安全耐受。
肝癌免疫治疗2.0时代,PD-1/PD-L1抗体联合抗血管生成再添新数据
继研究(阿替利珠单抗+贝伐珠单抗,III期)和-524研究(帕博利珠单抗+仑伐替尼,1b期)结果公布后ci524,PD-1/PD-L1抗体联合抗血管生成药物正在成为HCC具有前景的免疫联合治疗模式。今年ESMO上有多项PD-1/PD-L1抗体联合抗血管生成药物治疗晚期HCC的壁报展示。

上述研究虽然选择了不同的PD-1/PD-L1抗体和靶向药物,但在研究设计方面大体上都遵循了比较传统的设计方法(参考研究和-524研究)。现将上述研究的部分有效性和安全性数据汇总如下:
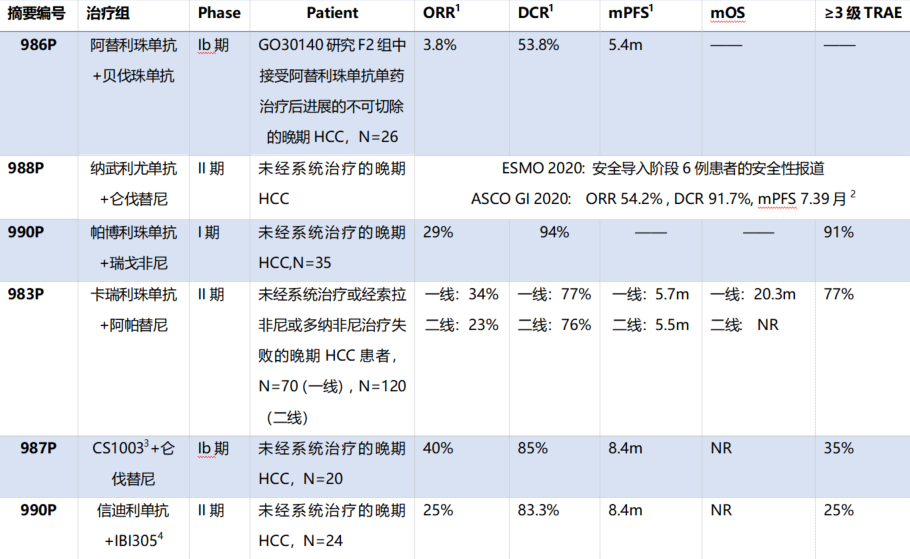
1. 根据 V1.1标准评估
2. 2020 ASCO GI, 513, 第二部分数据
3. 是一种人源化IgG4抗PD-1单克隆抗体(mAb)
4. 是一种贝伐珠单抗类生物药,与在药代动力学和疗效方面相似,已被国家药监局批准。
5. NR:未达到
生物标记物检测助力肝癌治疗,探索之路任重道远
998P - The with (HP) to (ICIs) in (HCC)
既往报告表明,MDM2/MDM4扩增(amp)、EGFR突变、突变、/B基因丢失和含CCND1、FGF3、FGF4和FGF19的11q13区域amp是多种癌症中与超进展(HP)相关的生物标志物。因此,对HCC这些基因的研究可能有助于避免HP发生。对1292例中国HCC接受ICI治疗患者的肿瘤组织和匹配的血液样本进行450个癌症相关基因的靶向深度测序,随后分析HP相关基因组改变,发现有202例(15.6%)患者出现HP相关基因改变。其中,分别在6例(0.46%)、16例(1.24%)、13例(1.01%)、58例(4.49%)和118例(9.13%)患者中发现了MDM2/MDM4 amp、EGFR改变、改变、/B基因丢失和11q13 amp。中位肿瘤突变负荷为6.3 muts/Mb(范围为0-554.5 muts/Mb),中位年龄为55岁(范围为7-87岁)。改变与显著高于野生型病例的年龄相关(中位年龄:60岁vs 55岁;P = 0.0096)。在11q13扩增亚组中,Ⅲ~Ⅳ期患者频率明显高于Ⅰ~Ⅱ期(36.2%vs 19.4%,P = 0.0048)。因此,在指导治疗方案和ICI治疗时,可能需要应用全面的基因组分析伴随诊断。
刘秀峰教授点评
今年ESMO唯一一项口头报告来自中国(981O),延续了中国研究者的地位,在肝癌系统治疗领域我国学者可谓正处于引领地位。对于不可切除了的大肝癌患者,HAIC组无论在ORR、PFS还是OS都显示了明显的优势,值得注意的是这组患者属于BCLC A或B,并没有大血管侵犯和远处转移,原本指南推荐是接受TACE。本项III期研究的结果颠覆了我们的传统观点,对TACE治疗提出了严峻的挑战,有可能改写中国的指南或规范,符合中国肝癌患者的生物学特征。对于在中国地区进行的多中心III期临床研究,能否推广到全球,值得关注。
另一项有关HAIC的II期研究来自北大肿瘤医院介入科团队。针对门静脉主干(Vp3/4)的初治肝癌患者,采用HAIC联合索拉非尼对比索拉非尼,灌注方案同样采取方案。结果联合组的获益显著,OS、ORR和PFS都明显延长。本项研究专门针对Vp3/4的中国患者,实际上与前一项口头报告不同,本组患者已届BCLC C期,但病灶局限于肝内,采取这样的联合模式意义重大。相信在不久的将来会改写以分期为指导的治疗流程,同时与现阶段的系统治疗比较,假设在HAIC的基础上联合免疫治疗,结果会如何?
983P、986-991P延续了免疫治疗的2.0版本时代,不同的免疫检查点抑制剂,不同的抗血管生成剂,疗效都在20%以上,其中中国特色的“双艾”组合在一线治疗的ORR为34%,同样来自中国的双药组合“信迪利单抗+”ORR为25%;在免疫联合的领域,也看到了瑞戈非尼的身影,瑞戈+K药的ORR为29%;作为早II期研究ORR最高的属O药联合仑伐,达到54.2%。自去年结果公布以后,免疫联合抗血管生成的治疗模式如雨后春笋,在晚期肝癌的系统治疗领域遍地开花,但这些早II期的喜人结果如何复制到III期临床,如何复制到中国肝癌患者的临床实践中,值得关注。的前期在今年的ESMO上的壁报986P,可能关注的不多。笔者认为可能具有一定的意义或市场,原因是这个F2组的病例来自阿替利珠单抗单药进展后转入阿替利珠单抗联合贝伐珠单抗,取得了3.8%的ORR,结果并不惊艳,病例数也很少,但可能直面了一个问题:PD-(L)1单抗耐药或进展后的治疗决策。
随着免疫检查点抑制剂的广泛应用,超进展的概念进入了大家的视野。超进展是相对于“进展”而言,通常是指肿瘤反常的加速生长,目前尚无标准的定义。超进展到底是由潜在的肿瘤生物学还是药物治疗影响所驱动的,目前还无法得出明确的结论。但是无论如何,出现超进展后建议应当立即中止免疫治疗,特别是如果患者出现相关症状的临床恶化。因此,如何预测超进展发生也是目前的热点话题,找到合适的预测标志物将能更好的指导免疫用药。近年来,一些学者均有文章发表,探索了一些可能的预测超进展的标志物:MDM2/MDM4扩增和EGFR突变,位于 11q13位点的一些基因扩增(如CCND1、FGF3、FGF4和FGF19等),中性粒细胞-淋巴细胞比率(NLR)升高(>4.125)等。今年ESMO上报道998P研究是目前中国HCC患者ICI治疗后超进展相关生物标志物突变情况探索的最大队列研究,我们期待有更多的学者加入这方面的研究,为超进展预测标志物增添更多证据。
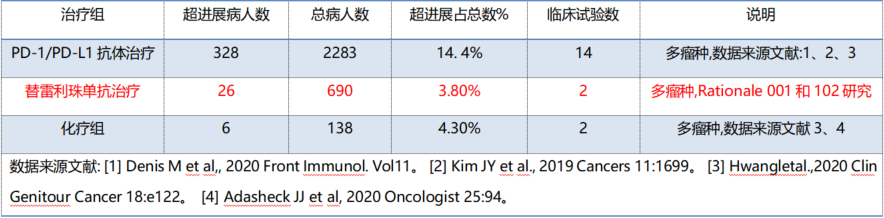
关于超进展的发生机制,目前相关文献探讨也甚少。2019 AACR会议上由M.C. 教授从病理学机理角度提出了三个导致超进展的充分必要条件:较多的肿瘤浸润 PD-1+T细胞,较多的肿瘤浸润巨噬细胞,能结合巨噬细胞 FcγR的PD-1 抗体。因此ci524,从理论上,对于PD-1抗体而言,如果对抗体结构进行改造,避免其巨噬细胞的FcγR结合,则似乎有可能会降低超进展的发生率。在目前的各类PD-1抗体中,替雷利珠单抗是一款修饰了抗体Fc段,可避免其Fc段与FcyR+效应细胞结合的抗体。结构的改造可降低ADCC/ADCP可能性,也避免了抗体依赖的吞噬作用和对巨噬细胞的诱导浸润。有文献汇总了各类PD-1抗体研究数据,报道了使用PD-1抗体后超进展的总体发生率约为14.4%。而汇总替雷利珠单抗和 102研究数据,超进展的发生率不到4%。当然这两项研究还只是I期数据,期待替雷利珠单抗的2期和3期数据的尽快公布,为超进展的学术探讨提供更多的数据。
限时特惠:本站持续每日更新海量各大内部创业课程,一年会员仅需要98元,全站资源免费下载
点击查看详情
站长微信:Jiucxh